阅尔基因高质量测序及数据分析助力临床新发现
不孕不育症影响全球15%的夫妇,其中男性因素约占50%。非梗阻性无精子症(Non-obstructive azoospermia, NOA)是男性不育中最严重的类型,其发病机制复杂,包括Y染色体微缺失、染色体异常、性腺功能低下、精索静脉曲张、睾丸肿瘤和性腺损伤药物等等。根据睾丸活检和病理分析,NOA可表现为唯支持细胞综合征(Sertoli cell only syndrome, SCOS)、生精阻滞(Maturation arrest, MA)和生精低下(Hypo-spermatogenesis, HS)。其中生精阻滞又可以进一步分为早期生精阻滞(精原细胞和精母细胞阻滞)和晚期生精阻滞(精子细胞阻滞)。与其他类型的NOA相比,生精阻滞患者睾丸体积及血清卵泡刺激素(FSH)水平相对正常,遗传变异发生频率更高。
近年来,一系列生精阻滞相关单基因致病突变已被发现,包括DMC1、STAG3、TEX11、SYCE1、TEX14、TEX15、XRCC2等,但绝大多数生精阻滞的遗传学因素仍有待揭示。近日,上海交通大学附属第一人民医院泌尿男科李铮教授团队与复旦大学附属妇产科医院、生殖与发育研究院张锋教授团队及上海科技大学生命科学院周智教授团队合作,对2个NOA家系及362例散发NOA患者进行遗传病因学研究,发现并鉴定了一种NOA致病新基因-SHOC1,该基因的双等位致病突变可通过影响减数分裂进程进而导致无精子症。上述相关研究成果“Bi-allelic SHOC1 loss-of-function mutations cause meiotic arrest and non-obstructive azoospermia”已发表于国际知名遗传学杂志《Journal of Medical Genetics》。

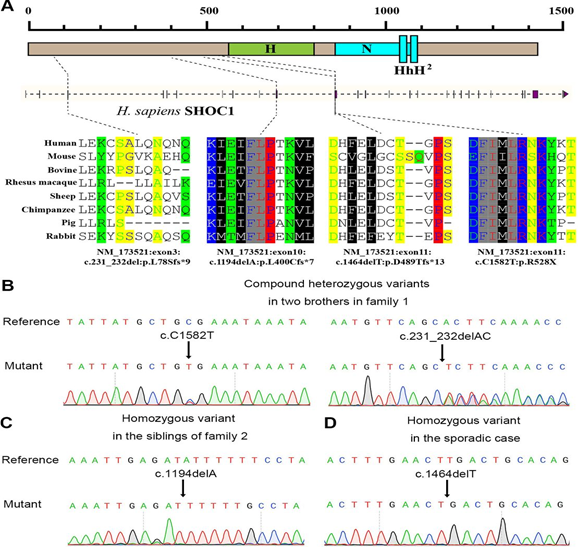
该研究入组了两个无精子症家系进行生精障碍新基因的鉴定。在家系1中,两个亲兄弟被临床诊断均为非梗阻性无精子症,且没有已知无精子症相关病因(染色体核型异常、Y染色体微缺失、精索静脉曲张等)。通过WES测序及Sanger测序证实兄弟二人均带有SHOC1复合杂合变异,包括父源的无义突变(c.C1582T, p.R528X)和母源的移码变异(c.231_232del, p.L78Sfs * 9)。在家系2中,先证者临床诊断为特发性非梗阻性无精子症,先证者之姐为原发性不孕患者。WES及后续Sanger测序证实先证者与其姐均为SHOC1纯合突变(c.1194delA, p.L400Cfs * 7)。进一步对362名特发性非梗阻性无精症患者进行遗传学筛查,鉴定SHOC1新功能缺失变异(c.1464delT, p.D489Tfs*13)。后续通过过碘酸希夫反应(PAS)、免疫荧光染色(IF)和染色体铺片实验分析评估精子发生停滞阶段,发现上述NOA患者精子发生均停滞在第一次减数分裂前期偶线期。
本文共同第一作者为上海交通大学附属第一人民医院姚晨成博士、杨超以及赵亮宇在读博士,共同通讯作者为上海交通大学附属第一人民医院泌尿男科李铮教授、复旦大学附属妇产科医院、生殖与发育研究院张锋教授及上海科技大学生命科学院周智教授。该篇报道与意大利佛罗伦萨大学团队同期证实SHOC1基因突变可以导致减数分裂障碍进而引起生精障碍,上述研究提示SHOC1基因致病模式符合常染色体隐性遗传模式,是非梗阻性无精子症单基因遗传学研究中的又一新发现。该研究基于上海交通大学附属第一人民医院泌尿男科前期构建的5800余例临床样本库,旨在为更多的男性不育患者找到病因,并在此基础上进一步深入研究,揭示单基因突变导致NOA的分子机制,实现无精子症患者的个体化精准治疗,构建新的生殖细胞体外培养体系,从而为该类患者生育自身健康子代奠定基础。
上海阅尔基因技术有限公司提供测序及数据分析协助。
关于阅尔基因
阅尔基因是一家领先的基因组学公司,是不孕不育基因检测领域的推动者和领先者,率先在国内对广泛存在的临床原因不明的男性不育、女性不孕、反复妊娠丢失等生育健康疾病开展基因检测,帮助在传统经验型诊疗方法下长期用药无效、多次辅助生殖失败、反复求诊无果的患者明确病因,精准治疗。阅尔基因在美国休斯顿,中国上海和中国苏州均设有分部。阅尔基因的愿景是提供负担得起的、及时的和准确的疾病状态信息,来实现精准医疗并改善患者预后。http://www.nuprobe.com.cn